Câu 14 : Đốt cháy hoàn toàn một hỗn hợp 2 hidrocacbon A , B là đồng đáng kể tiếp thu được thể tích hợi CO ; và H O là 12 : 23 . Xác định CTPT của hidrocabon và tinh % theo khỏi lượng mỗi hidrocacbon ?

Những câu hỏi liên quan
Đốt cháy hoàn toàn hỗn hợp Z gồm 2 hidrocacbon liên tiếp trong dãy đồng đẳng thu được 48,4g CO2 và 29,7g H2O. Xác định CTPT và tính phần trăm khối lượng của mỗi hidrocacbon
\(n_{CO_2}=\dfrac{48,4}{44}=1,1\left(mol\right)\\ n_{H_2O}=\dfrac{29,7}{18}=1,65\left(mol\right)\\ Vì:n_{H_2O}>n_{CO_2}\Rightarrow hhZ:hh.ankan\\ CTTQ:C_aH_{2a+2}\\ Ta.có:1< \dfrac{n_{CO_2}}{n_{H_2O}}=\dfrac{1,65}{1,1}=1,5< 2\\ \Rightarrow hh.Z:50\%V_{CH_4},50\%V_{C_2H_6}\\ \Rightarrow\%m_{\dfrac{CH_4}{hhZ}}=\dfrac{16}{16+28}.100\approx36,364\%\\ \Rightarrow\%m_{\dfrac{C_2H_6}{hhZ}}\approx63,636\%\)
Đúng 4
Bình luận (0)
Đốt cháy hỗn hợp hai hidrocacbon đồng đẳng kế tiếp nhau thu được 11.7g H2O và 17.6g CO2.Xác định CTPT của hai hidrocacbon trên.Tính % khối lượng mỗi ankan trong hỗn hợp.?
\( n_{H_2O} = \dfrac{11,7}{18} = 0,65\ mol\\ n_{CO_2} = \dfrac{17,6}{44} = 0,4\ mol\\ \Rightarrow Hidrocacbon :\ C_nH_{2n+2}\\ n_{hidrocacbon} = n_{H_2O} - n_{CO_2} = 0,65 - 0,4 = 0,25(mol)\\ \Rightarrow n = \dfrac{n_{CO_2}}{n_{hidrocacbon}} = \dfrac{0,4}{0,25} = 1,6\\ 1< n=1,6<2\Rightarrow Hidrocacbon:\ CH_4,C_2H_6\\ n_{CH_4} = a\ mol ; n_{C_2H_6} = b(mol)\\ \Rightarrow a + b = 0,25 ; n_{CO_2} =a + 2b = 0,4\\ \Rightarrow a = 0,1 ; b = 0,15\\ \Rightarrow \%m_{CH_4} = \dfrac{0,1.16}{0,1.16+0,15.30}.100\% = 26,23\%\)
\(\%m_{C_2H_6} = 100\% - 26,23\% = 73,77\%\)
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn hỗn hợp A gồm 1 hidrocacbon ở thể khí và oxi dư thu dduocj hỗn hợp B có thành phần thể tích là 30%co2 20%h2o 50%o2 xác định ctpt của h-c
\(Coi\ n_B = 1(mol) \\ n_{CO_2} = 1.30\% =0,3(mol) ; n_{H_2O} = 1.20\% = 0,2(mol)\\ A: C_nH_{2n+2-2k}\\\ n_C = n_{CO_2} = 0,3(mol)\\ n_H = 2n_{H_2O} = 0,4(mol)\\ Ta có : \dfrac{n}{2n+2-2k} = \dfrac{0,3}{0,4}\\ \Leftrightarrow 0,4n = 0,6n + 0,6 - 0.6k\\ \Leftrightarrow 0,6k -0,2n = 0,6\\ \Leftrightarrow 6k - 2n = 6\)
Với k = 1 thì n = 0(loại)
Với k = 2 thì n = 3(chọn)
Với k = 3 thì n = 6(chọn)
.....
Vậy hidrocacbon có thể là : \(C_3H_4 ; C_6H_8,...\)
Đúng 2
Bình luận (0)
\(Coi\ n_B = 1(mol)\\ \Rightarrow n_{CO_2} = 1.30\% = 0,3(mol) ; n_{H_2O} = 20\% = 0,2(mol) ; n_{O_2} = 50% = 0,5(mol)\)
Vì \(n_{CO_2} > n_{H_2O} \Rightarrow A: C_nH_{2n-2}\)
\(n_A = n_{CO_2} - n_{H_2O} = 0,3 - 0,2 = 0,1(mol)\\ \Rightarrow n = \dfrac{n_{CO_2}}{n_A} = \dfrac{0,2}{0,1} = 2\\ CTPT\ A: C_2H_2\)
Đúng 1
Bình luận (2)
Đốt cháy hoàn toàn hh X gồm 2 hidrocacbon A (CnH2n-2) và B (CmH2m) thu được 15,68 lít CO2 ở đktc và 14,4 gam H2O. Biết X chiếm thể tích là 6,72 lít ở đktc. Xác định tp % thể tích của hỗn hợp X, xác định CTPT của A,B
đốt cháy hoàn toàn hỗn hợp A gồm 1 hidrocacbon ở thể khí và oxi dư thu dduocj hỗn hợp B có thành phần thể tích là 30%co2 20%h2o 50%o2 xác định ctpt của h-c
Hỗn hợp khí X gồm 2 hidrocacbon A và B là đồng đẳng kế tiếp nhau. Đốt cháy X với 64 gam O2 (dư) rồi dẫn sản phẩm qua bình đựng Ca(OH)2 dư thu được 100g chất tủa. Khí thoát ra khỏi bình có thể tích 11,2 lít ở 0 độ C và 0,4 atm. Xác định CTPT của A và B
Ta có: \(n_{O_2\left(banđau\right)}=\dfrac{62}{32}=2\left(mol\right)\)
\(n_{CO_2}=n_{CaCO_3}=\dfrac{100}{100}=1\left(mol\right)\)
Khí thoát ra khỏi bình là O2 dư.
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{pV}{RT}=\dfrac{0,4.11,2}{0,082.273}=0,2\left(mol\right)\)
\(\Rightarrow n_{O_2\left(pư\right)}=2-0,2=1,8\left(mol\right)\)
BTNT O, có: \(2n_{O_2\left(pư\right)}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=2.1,8-2.1=1,6\left(mol\right)\)
Vì đốt cháy 2 hiđrocacbon thu được nH2O > nCO2 nên A và B là ankan.
⇒ nankan = 1,6 - 1 = 0,6 (mol)
Gọi CTPT chung của A và B là \(C_{\overline{n}}H_{2\overline{n}+2}\)
\(\Rightarrow\overline{n}=\dfrac{1}{0,6}=1,667\)
Vậy: A và B là CH4 và C2H6.
Bạn tham khảo nhé!
Đúng 1
Bình luận (0)
Câu 30: Đốt cháy hoàn toàn 1,12 lít ( đktc) một hidrocacbon A, sau phản ứng thu được 4,48 lít CO;(đktc) và 3,6 gam H₂O a) A thuộc dãy đồng đẳng nào, tìm CTPT của A? b) xác định CTCT đúng của A, biết A cộng hợp với HBr tạo 1 sản phẩm duy nhất?
a, Ta có: \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
⇒ nCO2 = nH2O → A thuộc dãy đồng đẳng của anken.
Gọi CTPT của A là \(C_nH_{2n}\)
\(n_A=\dfrac{1,12}{22,4}=0,05\left(mol\right)\Rightarrow n=\dfrac{n_{CO_2}}{n_A}=4\)
Vậy: A là C4H8.
b, A cộng HBr tạo sản phẩm duy nhất.
→ \(CH_3-CH=CH-CH_3\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn hỗn hợp 2 hidrocacbon (phân tử khối hơn kém nhau 14 đvC), thu được 5m (g) CO2 và 3m (g) H2O. CTPT của 2 hidrocacbon trên là: A. C3H8, C3H6 B. C2H6, C3H8 C. C2H2, C3H4 D. C3H6, C4H6
Đọc tiếp
Đốt cháy hoàn toàn hỗn hợp 2 hidrocacbon (phân tử khối hơn kém nhau 14 đvC), thu được 5m (g) CO2 và 3m (g) H2O. CTPT của 2 hidrocacbon trên là:
A. C3H8, C3H6
B. C2H6, C3H8
C. C2H2, C3H4
D. C3H6, C4H6
Đáp án B
Gọi công thức chung của 2 hidrocacbon là C x ' H y ' ( với x', y' lần lượt là số nguyên tử C trung bình và số nguyên tử H trung bình).
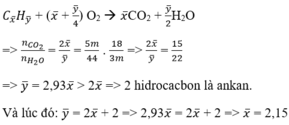
![]()
Đúng 0
Bình luận (0)
Đốt cháy hoàn toàn một hidrocacbon A. Thu được 13.2g CO2 và 5.4g H2O. Biết khối lượng mol của A là 28g. Hãy xác định CTPT của A
Help me !!!
Ta có: \(n_{CO_2}=\dfrac{13,2}{44}=0,3\left(mol\right)=n_C\)
\(n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\Rightarrow n_H=0,3.2=0,6\left(mol\right)\)
Giả sử: CTPT của A là CxHy
⇒ x : y = 0,3 : 0,6 = 1 : 2
⇒ CTĐGN của A là (CH2)n
Mà: MA = 28 (g/mol)
\(\Rightarrow n=\dfrac{28}{12+2}=2\)
Vậy: A là C2H4.
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)
Theo gt ta có: $n_{CO_2}=0,3(mol);n_{H_2O}=0,3(mol)$
Bảo toàn nguyên tố C và H ta có: $n_{A}=0,3.12+0,3.2=4,2(g)$
$\Rightarrow n_{A}=0,15(mol)$
Chia tỉ lệ số mol C và H cho mol A ta tìm được A là $C_2H_4$
Đúng 0
Bình luận (0)


















